코로나19 치료제 렘데시비르 미국 FDA 긴급 승인
미국 식품의약국(FDA)은 1일(현지시간) 신종 코로나바이러스 감염증(코로나19) 치료제로 기대되는
렘데시비르에 대해 긴급사용을 승인했다고 로이터통신 등이 보도했습니다.
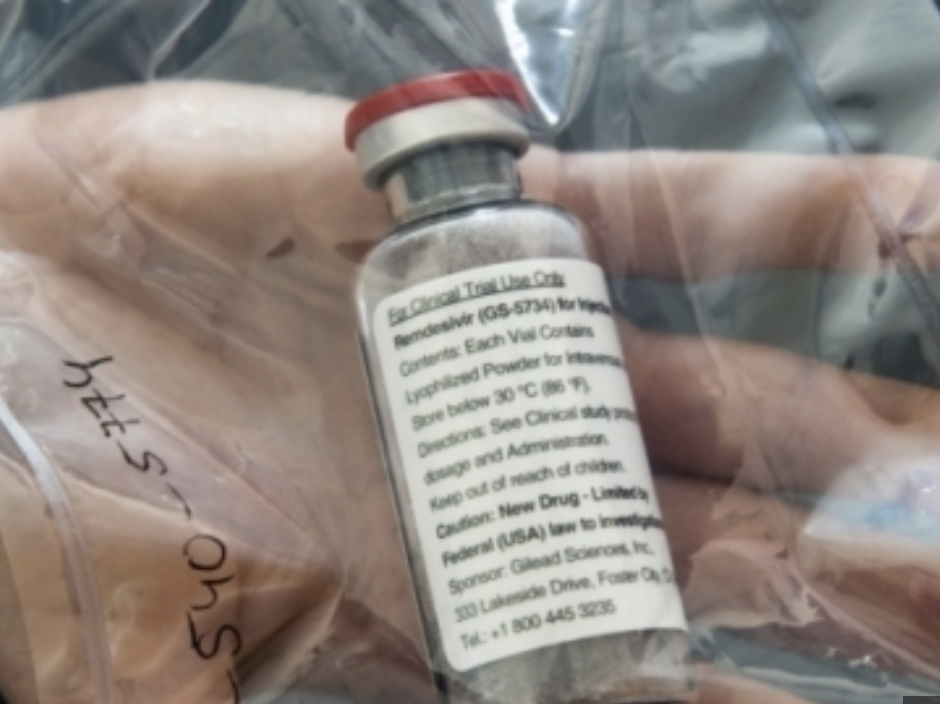
FDA는 이날 성명에서 렘데시비르가 호흡 장애로
인공호흡기를 필요로 하는 코로나19 중증 입원 환자를 위해 특별 지정될 것이라고 밝혔습니다.
렘데시비르는 제약회사 길리어드사이언스가
에볼라 치료제로 개발했었지만 코로나19 양성으로
입원한 환자를 대상으로 했었던 임상시험에서
긍정적인 결과가 나와 큰 관심을 받은바 있습니다.
도널드 트럼프 미국 대통령도 백악관에서 길리어드사의 대니얼 오데이 최고경영자(CEO), 스티븐 한 FDA 국장과 함께 한 자리에서 이같은 소식을 알렸습니다.

AP통신은 렘데시비르가 코로나19 극복을 돕는 것으로 나타난 최초의 약이라고 평가했습니다.
FDA의 긴급사용 승인은 연구가 진행 중인 상황에 취할 수 있는 조처로, 정식 사용허가와는 다릅니다.
다만 긴급사용 승인이 나면 처방은 가능합니다.
긴급사용 승인은 허가받은 대체 약이 없다는 뜻으로, 치료제가 전혀 없는 것보다는 낫다는 의미라는 겁니다.
미국 정부가 후원한 연구 예비 결론에 따르면 렘데시비르는 코로나19로 입원한 환자의 회복 기간을 31% 평균적으로 약 4일 단축하는 것으로 나타났습니다.
지금까지 임상시험 중 가장 큰 대규모인
1063명의 환자를 대상으로 시행되었으며, 효과를 엄격하게 평가할 수 있도록 일반적 치료를 받은 그룹과 비교 실험 또한 진행했습니다.
일반적 치료를 받은 환자들은 퇴원까지 평균 15일이 걸렸지만 렘데시비르 처방을 받은 이들은 11일이 소요된 것으로 알려졌습니다.
FDA는 안전과 효과에 관해 알려진 정보가 제한적이지만 효능은 보장된다고 안내했습니다.
렘데시비르의 부작용으로는 간의 염증, 투약방법에 따른 메스꺼움과 구토, 식은땀, 저혈압을 유발할 수 있습니다.
하지만 복용과 안전에 관련한 자료가 의사와 환자에게 제공될 것이라고 FDA는 설명했습니다.
'#News' 카테고리의 다른 글
| 고성산불 진화 완료! 인명피해는? (0) | 2020.05.03 |
|---|---|
| 고성군 산불 피해 봉사활동 안내. (0) | 2020.05.02 |
| 중앙일보 김정은 사망 예비기사 30초 노출후 삭제(기사내용첨부) (0) | 2020.05.02 |
| 사망설 김정은 건재한 모습 공개 어제 비료공장 준공식 참석(+사진추가) (0) | 2020.05.02 |
| CNN 인도네시아 김정은 건강 이상설 뉴스에 현빈 사진사용 사과 (0) | 2020.05.02 |








